Bienvenido a Justin Stindt Consultants, su agencia dedicada a programas de acceso temprano en Alemania. En el cambiante panorama médico alemán, tanto el uso compasivo de los medicamentos como la ‘Prueba controlada por solictud’ (Antragsgesteuerte Erprobung) para los dispositivos médicos ofrecen una vía prometedora para medicamentos y tecnologías innovadores que apuntan a una entrada acelerada al mercado. Nuestro equipo internacional de expertos y consultores está listo para ayudarlo a navegar este complejo proceso. Como agencia de consultoría global, entendemos los matices de los estrictos criterios de la agencia federal de medicamentos y dispositivos médicos de Alemania (Bundesinstitut für Arzneimittel und Medizinprodukte – BfArM), el instituto federal alemán de vacunas y biomedicinas (Paul-Ehrlich-Institut – PEI), y el comité federal conjunto (Gemeinsamer Bundesausschuss, G-BA). Confíe en nuestra experiencia para articular los beneficios únicos de su producto, garantizando una aplicación optimizada que se alinee con las expectativas de la BfArM, el PEI, y el G-BA. Confíe en Justin Stindt Consultants para ser su socio y maximizar el potencial de sus soluciones médicas innovadoras en Alemania.
Acelerando su acceso al mercado para tecnologías médicas innovadoras con la vía de "Prueba controlada por solicitud" (Antragsgesteuerte Erprobung) en Alemania
La “prueba controlada por solicitud” (Antragsgesteuerte Erprobung), un proceso iniciado por el G-BA, promete agilizar el acceso al mercado de tecnologías médicas innovadoras en la República Federal de Alemania. Las empresas de tecnologías médicas y diagnósticos pueden aprovechar esta vía para presentar solicitudes, que son evaluadas meticulosamente por el G-BA. Luego, las aplicaciones exitosas allanan el camino para que G-BA diseñe y ejecute ensayos clínicos personalizados.
A través de esta vía, se pueden poner a disposición tecnologías médicas innovadoras antes de que se tomen decisiones regulares de reembolso, lo que puede llevar muchos años. Por lo tanto, permite a los pacientes beneficiarse antes de las posibles ventajas terapéuticas de las tecnologías médicas. Además, generar datos positivos a través de esta vía mejora las posibilidades de las empresas de obtener reembolso por sus productos, aumentando la entrada al mercado y el potencial de adopción.

Justin Stindt Consultants es una agencia de consultoría líder especializada en la “prueba controlada por solicitud” (Antragsgesteuerte Erprobung). Nuestro dedicado equipo de consultores y especialistas lo ayudará a articular el beneficio adicional de su producto en el dosier de “prueba controlada por solicitud” (Antragsgesteuerte Erprobung). El proceso general es complejo, pero con nuestro equipo de expertos a su lado, sus responsabilidades principales terminan después del envío de la solicitud.
Obtenga acceso al mercado en Alemania antes de tener una autorización de comercialización, gracias al programa de ‘Uso Compasivo’ (Härtefall)
- El PEI es la autoridad competente en materia de sueros, vacunas, preparados sanguíneos, tejidos y preparados de tejidos, alérgenos, medicamentos de terapia avanzada, medicamentos xenógenos y componentes sanguíneos genéticamente modificados.
- BfArM es la autoridad competente para todos los demás medicamentos.
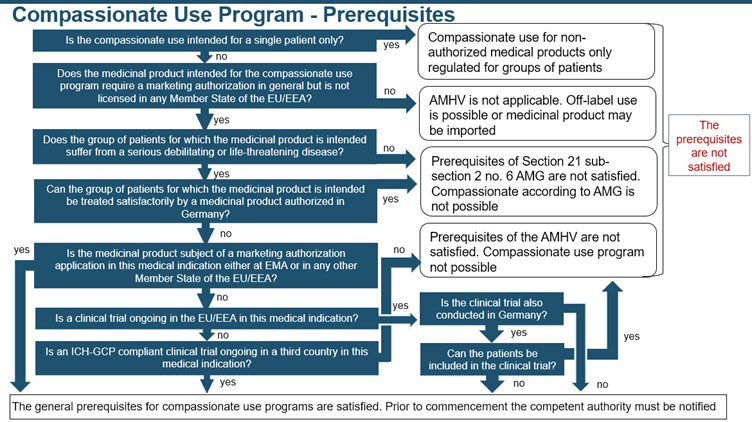
Este programa facilita la disponibilidad temprana del medicamento antes de obtener la autorización de comercialización, permitiendo a los pacientes acceder antes a sus beneficios. Además, el apoyo adicional proporcionado a través de la generación de datos positivos puede fortalecer los argumentos de la empresa para obtener la autorización de comercialización. Se sigue el siguiente árbol de decisiones para evaluar si se cumplen los requisitos previos:
Si su empresa está considerando esta ruta, Justin Stindt Consultants está listo para ayudarlo. Navegar por los diversos documentos requeridos puede ser complejo, pero con nuestro equipo experimentado, contará con soporte dedicado en cada paso del camino.
Nuestra agencia ha sido seleccionada por muchas empresas farmacéuticas, biotecnológicas y de tecnologías médicas como proveedor de servicios preferido para redactar las solicitudes de acceso temprano en Alemania. Nuestra empresa cuenta con hablantes nativos de alemán con amplia experiencia tanto en la industria como en agencias de consultoría y un historial exitoso de dosieres de acceso temprano que condujeron al acceso temprano en Alemania.
MEJORAR EL ACCESO AL MERCADO CON LOS CONSULTORES DE JUSTIN STINDT: EXPERIENCIA EN INVESTIGACIÓN DE ANÁLOGOS, EVALUACIÓN DE PRECIOS Y CONSULTAS SOBRE EL CUIDADO DE LA SALUD EN ALEMANIA

En Justin Stindt Consultants, entendemos las complejidades de este complejo proceso y estamos aquí para apoyarlo en cada paso del camino. Antes de emprender este viaje, recomendamos una reunión de asesoramiento con el G-BA para evaluar los requisitos de evidencia y evaluar las posibilidades de éxito. Nuestro equipo de expertos tiene una amplia experiencia en la creación de solicitudes de asesoramiento de conformidad con el artículo 137e SGB V. Nuestra firma de consultoría brinda una evaluación integral de los requisitos, respaldo basado en evidencia para respaldar su posición, y preparación y participación en profundidad en las consultas con el G-BA.
Al asociarse con Justin Stindt Consultants como su agencia, obtiene acceso a nuestra riqueza de conocimientos y experiencia, lo que le permite enviar sus solicitudes con confianza y navegar por las complejidades del camino de «Prueba controlada por solicitud» (Antragsgesteuerte Erprobung). Sus responsabilidades principales finalizan después del envío de la solicitud; nosotros nos encargamos del resto. Seamos su agencia de confianza para acelerar su viaje de acceso al mercado en Alemania.
Si está buscando un proveedor que respalde sus programas de acceso temprano en Alemania, seleccione un proveedor de servicios que haga un esfuerzo adicional para permitir el acceso temprano para su producto. Más que un simple proveedor de solicitudes, Justin Stindt Consultants se asociará con usted y puede brindarle soporte de servicio completo, incluidas las interacciones con las autoridades.
Dé el primer paso para asegurar el acceso al mercado para sus tecnologías médicas innovadoras. Contáctenos hoy para saber cómo podemos adaptar nuestros servicios para satisfacer sus necesidades únicas y hacer realidad sus objetivos de reembolso.
Conozca a uno de nuestros expertos en programas de acceso temprano en Alemania

Póngase en contacto con nuestro experto
Conecte con nuestro equipo
Nuestros experimentados especialistas en acceso a los mercados están a un solo clic de distancia
TESTIMONIOS DE CLIENTES